摘要:研究人员开展发现 SLC6A14 通过组蛋白磷酸化调控巨噬细胞炎症,为炎症性疾病治疗提供新靶点。
在人体的免疫系统中,巨噬细胞就像一群时刻警惕的卫士,它们是免疫系统的 “先遣部队”,一旦有外敌入侵,巨噬细胞会迅速做出反应。在正常情况下,它们能根据不同的环境需求,分泌不同的细胞因子。比如,当有病原体来袭时,炎症性巨噬细胞会分泌白细胞介素 - 1β(IL-1β)等促炎细胞因子来清除病原体;而在组织受损时,抗炎性巨噬细胞则会分泌 IL-10 等抗炎因子来修复组织。然而,巨噬细胞的 “工作” 一旦出现差错,就会引发各种健康问题。像是在败血症、感染诱导的炎症性疾病中,巨噬细胞的表型转换出现缺陷,炎症性属性持续激活,给患者带来极大的痛苦。
同时,巨噬细胞的极化过程需要能量、物质合成等多方面的支持,这就离不开细胞的代谢重编程,而氨基酸在这个过程中扮演着重要角色。溶质载体(SLC)家族 6(SLC6)负责调节巨噬细胞对氨基酸的摄取,但是 SLC6 家族成员究竟如何影响巨噬细胞的极化和炎症反应,在之前还是一个未解之谜。
 图1 天冬酰胺转运蛋白通过组蛋白磷酸化支持巨噬细胞炎症
图1 天冬酰胺转运蛋白通过组蛋白磷酸化支持巨噬细胞炎症为了揭开这个谜团,来自华南农业大学的研究人员开展了深入的研究。他们发现 SLC6A14 在炎症性巨噬细胞中起着关键作用,通过一系列复杂的机制调控炎症反应。这一研究成果发表在《SCIENCE ADVANCES》上,为炎症性疾病的治疗开辟了新的方向。
研究人员在开展研究时,用到了多种关键技术方法。在细胞和动物模型方面,他们分离培养了原代腹腔巨噬细胞(PEMs)、骨髓来源的巨噬细胞(BMDMs)、肺泡巨噬细胞(AMs)等,还构建了 Slc6a14fl/flLyz2Cre基因敲除小鼠模型。实验检测技术上,运用蛋白质免疫印迹(Western blot)检测蛋白表达,实时荧光定量聚合酶链式反应(RT-qPCR)分析基因表达,酶联免疫吸附测定(ELISA)检测细胞因子水平,以及免疫荧光、透射电镜等技术进行观察分析 。
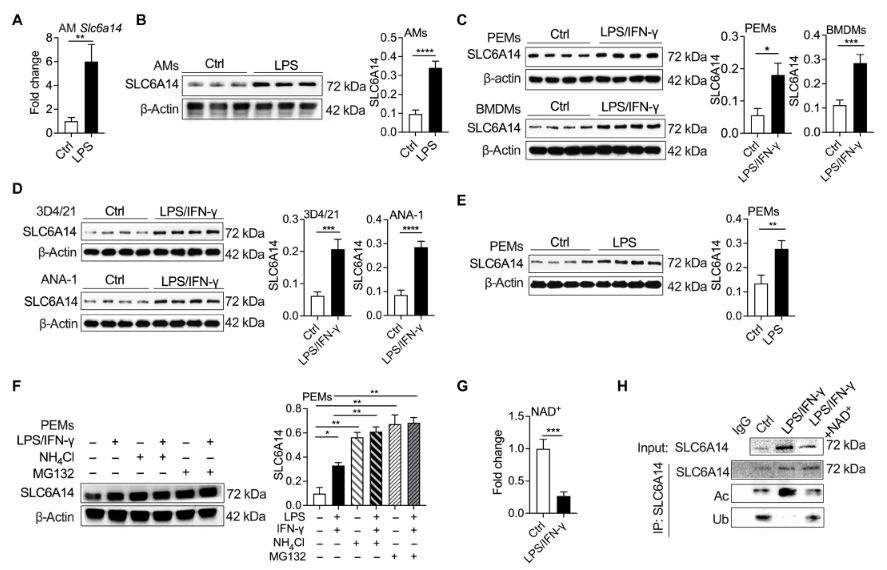 图2 NAD+介导的乙酰化促进SLC6A14的表达
图2 NAD+介导的乙酰化促进SLC6A14的表达下面来看具体的研究结果:
SLC6A14 与巨噬细胞介导的肺炎相关:研究人员分析转录组数据发现,SLC6A6 和 SLC6A14 在健康和感染肺部均高表达,且 SARS-CoV-2 等病原体感染会增加人肺中 SLC6A14 的表达。对小鼠的研究也证实,脂多糖(LPS)处理可使肺泡巨噬细胞中 SLC6A14 的 mRNA 和蛋白表达增加,表明 SLC6A14 在肺炎炎症性巨噬细胞中高表达。
NAD+介导的乙酰化增强炎症性巨噬细胞中 SLC6A14 的丰度:在体外实验中,用 LPS 加干扰素 -γ(IFN-γ)刺激巨噬细胞,发现炎症性 PEMs、BMDMs 等细胞中 SLC6A14 的蛋白表达增加。研究还发现,蛋白降解途径影响 SLC6A14 的丰度,NAD+通过调节蛋白乙酰化和泛素化,增加炎症性巨噬细胞中 SLC6A14 的丰度。
SLC6A14 抑制通过 NLRP3 炎性小体限制 IL-1β 分泌:使用 SLC6A14 选择性抑制剂 α- 甲基 -(dl)- 色氨酸(α-MT)处理炎症性巨噬细胞,发现 α-MT 可抑制 IL-1β 和肿瘤坏死因子 -α(TNF-α)的分泌。进一步研究表明,α-MT 对 NF-κB 信号通路无影响,但可阻断 NLRP3 炎性小体的激活和组装,还能改变线粒体相关指标,说明 SLC6A14 抑制通过 NLRP3 炎性小体限制 IL-1β 分泌。
SLC6A14 抑制通过天冬酰胺降低 NLRP3 炎性小体激活:α-MT 处理炎症性巨噬细胞后,细胞内多种氨基酸水平下降,但 12 小时后多数氨基酸恢复,只有天冬酰胺和丙氨酸未恢复。实验发现,补充天冬酰胺可恢复 IL-1β 分泌和 NLRP3 炎性小体激活,而补充丙氨酸则无此效果,表明 SLC6A14 抑制通过天冬酰胺降低 NLRP3 炎性小体激活。
SLC6A14 抑制通过 CCNO 抑制 MAPK 信号通路:RNA 测序分析发现,SLC6A14 抑制影响 MAPK 信号通路。免疫印迹实验表明,SLC6A14 抑制可抑制 MAPK 信号通路的活性。进一步研究发现,Ccno 基因在 SLC6A14 介导的 IL-1β 分泌中起重要作用,沉默 Ccno 基因可激活 MAPK 信号通路和 NLRP3 炎性小体,增加 IL-1β 分泌,说明 SLC6A14 通过 CCNO-MAPK 信号调节 NLRP3 炎性小体介导的 IL-1β 分泌。
SLC6A14 抑制通过核 LKB1 促进 CCNO 转录:研究人员推测 SLC6A14 介导的天冬酰胺摄取通过核肝激酶 B1(LKB1)介导的组蛋白磷酸化调节 Ccno 转录。实验结果显示,SLC6A14 抑制促进 LKB1 核保留,增加组蛋白 3 pS10/28 丰度和 Ccno 翻译,而补充天冬酰胺则会逆转这些变化。沉默 Lkb1 基因可促进 IL-1β 分泌,支持了上述推测,即 SLC6A14 抑制通过核 LKB1 介导的组蛋白磷酸化促进 Ccno 转录。
SLC6A14 缺陷减少巨噬细胞中 IL-1β 分泌:研究人员构建了巨噬细胞特异性 Slc6a14 缺陷小鼠模型,发现该模型中炎症性巨噬细胞的天冬酰胺水平降低,核 LKB1、组蛋白 3 pS10/28 和 CCNO 丰度增加,MAPK 和 NLRP3 炎性小体激活减少,IL-1β 分泌降低。补充天冬酰胺或沉默 Lkb1 基因可逆转这些变化,进一步证实 SLC6A14 通过核 LKB1 依赖性磷酸化介导炎症性巨噬细胞中 IL-1β 的分泌。同时,研究还确定了 SLC6A14 的 K636 乙酰化抑制其在炎症性巨噬细胞中的泛素化。
髓系 Slc6a14 缺失减轻 LPS 诱导的肺部炎症:在体内实验中,LPS 刺激可增加肺部巨噬细胞中 SLC6A14 的表达,抑制 CCNO 表达。髓系 Slc6a14 缺陷的小鼠在 LPS 诱导的肺部炎症模型中,存活率增加,肺部、血清和脾脏中的 IL-1β 产生减少,肺部炎症减轻,炎症性巨噬细胞比例降低,CCNO 表达增加,表明 SLC6A14 在体内调节巨噬细胞介导的肺部炎症。
综合研究结论和讨论部分的内容,此次研究意义重大。研究揭示了 SLC6A14 介导的天冬酰胺摄取通过组蛋白磷酸化调控巨噬细胞炎症的网络机制,SLC6A14 有望成为治疗肺炎等炎症性疾病的关键靶点。不过,研究也发现 SLC6 家族成员在不同免疫疾病中功能多样,炎症性巨噬细胞对 SLC6 底物选择的调节机制仍有待进一步研究。此外,LKB1 在其他细胞中的功能以及是否通过其他信号通路调节巨噬细胞功能也需要深入探索。但无论如何,这项研究为理解免疫细胞代谢与炎症反应的关系提供了新视角,为开发治疗炎症性疾病的新策略奠定了坚实基础。
参考资料
[1] Asparagine transporter supports macrophageinflammation via histone phosphorylation
 图1 天冬酰胺转运蛋白通过组蛋白磷酸化支持巨噬细胞炎症
图1 天冬酰胺转运蛋白通过组蛋白磷酸化支持巨噬细胞炎症