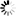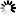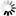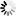硫酸软骨素(Chondroitin sulfate, CAS:9007-28-7)是一种天然的氨基多糖类物质,主要存在于人体的结缔组织、皮肤和眼睛等部位。硫酸软骨素是由重复的二糖单元构成的多糖链,这些二糖单元主要由葡萄糖醛酸和N-乙酰半乳糖胺组成。它通过一个糖链接区连接到核心蛋白的丝氨酸残基上。
硫酸软骨素可以从鲨鱼、牛、猪、鸡等动物的软骨中萃取得到,它在生物医药领域有着广泛的应用。
硫酸软骨素产品
英文名称:Chondroitin sulfate
CAS:9007-28-7
分子式: C13H21NO15S
分子量: 463.36854
保存条件:阴凉处
|
产品
|
CAS
|
级别
|
包装
|
|
硫酸软骨素
|
9007-28-7
|
食品级
|
1Kg; 25Kg
|
|
硫酸软骨素
|
9007-28-7
|
医药级
|
1Kg; 25Kg
|
硫酸软骨素功效
骨关节炎和其他关节疾病: 硫酸软骨素对于骨关节炎、风湿性关节炎、肩周炎、滑膜炎等疾病有一定的作用。它可以促进软骨细胞的代谢,改善关节软骨的血液循环,从而缓解关节炎症。同时还可以促进关节软骨的合成,改善关节软骨的质量。
促进伤口愈合: 硫酸软骨素具有促进伤口愈合的功效,可以加速伤口的修复过程。它能够促进肉芽的形成,同时也利用动物的粘多糖防止手术后的粘合。
改善关节问题: 硫酸软骨素对改善老年退行性关节炎、风湿性关节炎有一定的效果,可以改善关节问题。它能够保持体内水分,进行养分等的消化、吸收、搬运、新陈代谢等作用。
预防心脑血管疾病: 硫酸软骨素还可以促进血管新生,改善微循环,对于心脑血管疾病有一定的辅助作用。
缓解神经性和肌肉疼痛: 硫酸软骨素可以用于神经痛、神经性偏头痛、关节痛、关节炎,以及肩胛关节痛,还可以用于腹腔手术后的疼痛,缓解链霉素所引起的听觉障碍,以及各种噪音所引起的听觉困难、耳鸣等。
眼科应用: 硫酸软骨素在眼科中用于促进角膜水分代谢、改善微循环、保护角膜并促进角膜组织损伤修复。
食品应用
食品补充剂中硫酸软骨素的风险评估
评估了食品补充剂中硫酸软骨素的安全性和风险。硫酸软骨素是关节软骨的天然成分,常用于食品补充剂中。食品补充剂必须是安全的,不得对健康有害,且成分不应具有显著的药理作用。强调了食品补充剂的安全性和监管的重要性,保障消费者的健康。
海参硫酸软骨素多糖在缓解食物过敏中的作用
比较了海参硫酸软骨素(SCCS)与鲨鱼、牛和猪的硫酸软骨素在抗过敏活性方面的差异。
SCCS显著抑制了RBL-2H3细胞的脱颗粒,减轻了小鼠的过敏症状,并通过增加特定肠道菌群和短链脂肪酸的比例,促进黏蛋白2(MUC2)的分泌以及调节性T细胞的分化。本研究为深入了解SCCS在缓解食物过敏中的作用机制。
富含硫酸软骨素的鳐鱼糜罐头食品的制作工艺
开发了富含硫酸软骨素的鱼罐头(例如“白酱鳐鱼和鳕鱼”和“番茄酱鳐鱼和鳕鱼肉丸”),并介绍了相关制作工艺。每罐罐头食品中硫酸软骨素的含量为550至700毫克,保证了每日摄入量的78%至100%。采用红外热烫法去除鱼肉中的尿素,优化了罐头食品的配方和灭菌模式。该研究为开发富含硫酸软骨素的功能性食品提供了技术支持,并保证了产品的安全性和质量。
基于玉米醇溶蛋白的自组装复合纳米粒子作为姜黄素的运载载体
采用反溶剂沉淀法自组装制备了玉米醇溶蛋白和硫酸软骨素 (CS) 复合纳米粒子来负载姜黄素 (ZCCNPs)。研究表明,随着 CS 的增加,ZCCNPs 的结构由球形变为微聚集体,涉及氢键、静电和疏水作用。CS 提高了 ZCCNPs 的抗变性能力和姜黄素的包封率,最佳包封率为 91.97%。体外实验表明,ZCCNPs 提高了姜黄素对 HCT116 细胞的抗增殖活性和生物可及性,并且对 NCM460 细胞显示出良好的生物相容性。结果表明,CS 提高了载姜黄素纳米粒子的性能,使其在功能性食品中的应用前景广阔。
高效液相色谱法测定保健食品中的硫酸软骨素
建立了一种快速简便的高效液相色谱法测定保健食品中硫酸软骨素的方法。该方法在0.008~0.04 mg/mL范围内线性关系良好,平均回收率为98.5%~100.0%,RSD为0.6%。该方法可用于保健食品中硫酸软骨素的测定,具有快速、简便、准确和重现性好的优点,可以在实验室推广应用。
医药应用
硫酸软骨素 E 在血管生成中的作用
硫酸软骨素 E (CS-E) 是一种含有 E 型二糖单元的糖胺聚糖,其在N-乙酰半乳糖胺的 C-4 和 C-6 处硫酸化。CS-E 通过与核心蛋白共价连接,形成硫酸软骨素蛋白聚糖 (PG),这些PG可以分泌或与细胞质膜相关。含有 CS-E 的 PG 选择性地与生长因子和趋化因子相互作用,从而控制各种细胞和组织过程。血管生成在生理条件下受到严格调控,但在病理条件下可能失调,导致血管形成过量或不足。多种生长因子如血管内皮生长因子 A、成纤维细胞生长因子等协调血管生成,这些因子的功能可能受到含有 CS 的 PG 的影响。
脊髓损伤后硫酸软骨素的作用
脊髓损伤导致急性和慢性变化,最终形成神经胶质瘢痕。该瘢痕由成纤维细胞、巨噬细胞、小胶质细胞和反应性星形胶质细胞等组成,瘢痕内积聚的细胞外基质 (ECM) 分子,主要是硫酸软骨素蛋白聚糖 (CSPG),被认为抑制轴突再生。研究讨论了 CSPG 在损伤反应中的作用,特别是硫酸化糖胺聚糖 (GAG) 链如何通过与受体相互作用抑制可塑性和再生。理解 CSPG 在神经胶质瘢痕中的抑制作用,对于开发新疗法具有重要意义。
作为中枢神经系统损伤的新兴策略
硫酸软骨素蛋白聚糖 (CSPG) 是中枢神经系统 (CNS) 损伤后形成的神经胶质疤痕的主要成分,对轴突再生有抑制作用。中枢神经系统的愈合需要降解 CSPG 的糖胺聚糖骨架,以降低其抑制作用。本研究讨论了一些重要的再生方法,这些方法旨在克服 CSPG 引起的抑制屏障,从而促进 CNS 损伤后的修复。通过选择性降解 CSPG,可以促进神经突生长锥的扩展,从而提高轴突再生的能力。
作为多发性硬化症中白细胞浸润的新靶点
多发性硬化症导致中枢神经系统细胞外基质发生显著变化,特别是硫酸软骨素蛋白聚糖(CSPG)。利用实验性自身免疫性脑脊髓炎模型研究CSPG的作用,发现疾病高峰期时,小鼠脊髓中CSPG的4-硫酸化糖胺聚糖侧链和Versican V1核心蛋白上调,与炎症区域相对应。CSPG在炎症性血管周围袖带中强烈上调,这是免疫细胞进入中枢神经系统的关键门户。通过组织培养,发现CSPG上调了巨噬细胞中的促炎细胞因子和趋化因子,并提高了与白细胞穿越屏障相关的基质金属蛋白酶水平。在体外迁移实验中,CSPG也增强了巨噬细胞的迁移能力。此外,CSPG与四名多发性硬化症患者的炎症血管周围白细胞相关。因此,认为CSPG在多发性硬化症中促进了白细胞的活动和迁移,是减少炎症级联和临床严重程度的新靶点。
药物递送
硫酸软骨素功能化纳米粒子用于结肠巨噬细胞靶向药物输送
硫酸软骨素(CS)被结合到聚合物纳米颗粒(NPs)的表面,用于结肠巨噬细胞靶向药物输送。CS结合后的NPs(CS-NPs)平均直径为281 nm,尺寸分布单分散,表面带负电。CS-NPs显示出优异的生物相容性,并在Raw 264.7巨噬细胞中具有较高的细胞内化效率。CS-NPs在抑制脂多糖刺激的巨噬细胞分泌主要促炎细胞因子方面,显示出显著强于羧甲基纤维素功能化的CUR封装NPs(CUL-NPs)的能力。
硫酸软骨素功能化聚合物纳米粒子用于结肠癌靶向化疗
为解决结肠癌化疗药物靶向递送的问题,将喜树碱 (CPT) 负载到聚合物纳米颗粒 (NPs) 中,并用硫酸软骨素 (CS) 对其表面进行功能化。所得CS-CPT-NPs具有理想的流体动力学直径 (289 nm)、窄粒径分布 (多分散性指数 = 0.192) 和中性表面电荷。体外实验表明,CS表面功能化赋予NPs结肠癌靶向药物递送能力,并显著提高抗结肠癌活性和对结肠癌细胞的促凋亡作用。不同NPs对结肠肿瘤小鼠的研究表明,CS-CPT-NPs显示出比非靶向NPs更好的效果且无全身毒性。因此,CS-CPT-NPs有望成为结肠癌靶向化疗的有效药物递送系统。
硫酸软骨素杂交玉米醇溶蛋白纳米粒子用于多西紫杉醇的肿瘤靶向递送
硫酸软骨素(CS)与玉米醇溶蛋白(zein)结合形成杂交纳米粒子(zein/CS NPs),这些纳米粒子被开发用于多西他赛的靶向递送。zein/CS NPs 显示出更好的胶体稳定性,在血清中能保持初始大小 12 小时。CS 的预处理使 PC-3 细胞中 NPs 的摄取效率降低了 23%,表明 CS 参与了 CD44 介导的摄取机制。zein/CS NPs 的 IC50 值比游离多西他赛低 2.79 倍。近红外荧光成像证实,NPs 在 PC-3 异种移植小鼠中的肿瘤蓄积增强了 35.3 倍(与游离 Cy5.5 相比)。NPs 表现出更好的药代动力学特性,终末半衰期延长了 9.5 倍,抗肿瘤功效与泰索帝相当,全身毒性可忽略不计。
医用新材料
基于壳聚糖-硫酸软骨素的聚电解质复合物可有效治慢性伤口
使用壳聚糖 (CH) 和硫酸软骨素 (CS) 制备了聚电解质复合物 (PEC),通过质量源于设计 (QbD) 方法优化了其制造。制备的PEC表现出高膨胀性和孔隙率,不溶血,具有良好的血液相容性和低凝血指数,表现出对革兰氏阳性菌和革兰氏阴性菌的良好抗菌活性。细胞增殖研究显示,与对照组相比,用CH-CS PEC处理后细胞相容性良好,细胞密度几乎增加四倍。结果表明,CH-CS PEC具有良好的血液相容性、高抗菌效果,并通过刺激成纤维细胞生长促进伤口愈合,使其成为理想的伤口敷料材料。
用于骨再生的硫酸软骨素糖胺聚糖支架
将硫酸软骨素糖胺聚糖 (CS-GAG) 支架与临床标准的胶原海绵进行了比较,作为重组人骨形态发生蛋白 2 (rhBMP-2) 的递送载体。研究发现,与胶原海绵相比,CS-GAG 支架中 rhBMP-2 的释放时间更长。此外,插入间充质干细胞 (BMP-2 MSC) 的人 BMP-2 基因表达 rhBMP-2 的方法也显示了更长的释放时间。在用于治大鼠中具有挑战性的临界尺寸股骨缺损模型时,CS-GAG 支架中的 rhBMP-2 和 BMP-2 MSC 均诱导了与胶原海绵中的 rhBMP-2 相当的骨形成,以骨体积、强度和硬度来衡量。结果表明,CS-GAG 支架是一种有前途的运载工具,可用于控制 rhBMP-2 的释放并促进临界尺寸节段性骨缺损的修复。
胶原蛋白和硫酸软骨素功能化仿生纤维用于肌腱组织工程
通过同轴稳定喷射静电纺丝方法制造了高度对齐的聚 (L-乳酸) (PLLA) 纤维,其表面装饰有 1 型胶原蛋白 (COL1) 和硫酸软骨素 (CS)。研究发现,与普通 PLLA 纤维相比,仿生 COL1-CS/PLLA 纤维上的细胞扩散和增殖率更高。肌腱相关基因 scleraxis (SCX) 和 COL1 以及蛋白质肌腱调节蛋白 (TNMD) 的表达显著增加。机械刺激对 hMSC 的肌腱分化有协同作用,激活了 TGF-β 信号通路,促进了 hMSC 的肌腱分化。动物实验表明,COL1-CS/PLLA 支架促进了大鼠跟腱修复中的肌腱样组织再生。因此,这种仿生纤维可以作为功能性肌腱再生的有效支架系统。
参考信息:
1. Li, C., Tian, Y., Pei, J., Zhang, Y., Hao, D., Han, T., Wang, X., Song, S., Huang, L., & Wang, Z. (2023). Sea cucumber chondroitin sulfate polysaccharides attenuate OVA-induced food allergy in BALB/c mice associated with gut microbiota metabolism and Treg cell differentiation. Food & Function. https://doi.org/10.1039/d3fo00146f
2. Stellavato, A., Restaino, O. F., Vassallo, V., Finamore, R., Ruosi, C., Cassese, E., de Rosa, M., & Schiraldi, C. (2019). Comparative analyses of pharmaceuticals or food supplements containing chondroitin sulfate: Are their bioactivities equivalent? Advances in Therapy, 36(12), 3221-3237. https://doi.org/10.1007/s12325-019-01064-8
3. Raybulov, S., & Shokina, Y. (2020). Technology of minced fish canned food from thorny skate, enriched with chondroitin sulfate. KnE Life Sciences, 5(1), 819–835.
4. Caiyun, C., Weijiang, C., Hongbi, C., & XianBang, L. (2015). Determination of chondroitin sulfate in health food by high performance liquid chromatography. Journal of Food Safety and Quality, 6, 1913-1918. https://api.semanticscholar.org/CorpusID:101988539
5. Kastana, P., Choleva, E., Poimenidi, E., Karamanos, N., Sugahara, K., & Papadimitriou, E. (2019). Insight into the role of chondroitin sulfate E in angiogenesis. The FEBS Journal, 286(15), 1-15. https://doi.org/10.1111/febs.14830
6. Hussein, R. K., Mencio, C., Katagiri, Y., Brake, A. M., & Geller, H. M. (2020). Role of chondroitin sulfation following spinal cord injury. Frontiers in Cellular Neuroscience, 14. https://doi.org/10.3389/fncel.2020.00208
7. Mukherjee, N., Nandi, S., Garg, S., Ghosh, S., Ghosh, S., Samat, R., & Ghosh, S. (2020). Targeting chondroitin sulfate proteoglycans: An emerging therapeutic strategy to treat CNS injury. ACS Chemical Neuroscience. https://doi.org/10.1021/acschemneuro.0c00004
8. Stephenson, E., Mishra, M. K., Moussienko, D., Laflamme, N., Rivest, S., Ling, C.-C., & Yong, V. W. (2018). Chondroitin sulfate proteoglycans as novel drivers of leucocyte infiltration in multiple sclerosis. Brain, 141, 1094–1110.
9. Zhang, X., Ma, Y., Ma, L., Zu, M., Song, H., & Xiao, B. (2019). Oral administration of chondroitin sulfate-functionalized nanoparticles for colonic macrophage-targeted drug delivery. Carbohydrate Polymers, 223, 115126. https://doi.org/10.1016/j.carbpol.2019.115126
10. Zu, M., Ma, L., Zhang, X., Xie, D., Kang, Y., & Xiao, B. (2019). Chondroitin sulfate-functionalized polymeric nanoparticles for colon cancer-targeted chemotherapy. Colloids and Surfaces B: Biointerfaces, 177, 399-406.
11. Lee, H. S., Kang, N., Kim, H., Kim, D. H., Chae, J., Lee, W., ... Kim, D. D., & Lee, J. Y. (2021). Chondroitin sulfate-hybridized zein nanoparticles for tumor-targeted delivery of docetaxel. Carbohydrate Polymers, 253, 117187.
12. Sharma, S., Swetha, K., & Roy, A. (2019). Chitosan-chondroitin sulfate based polyelectrolyte complex for effective management of chronic wounds. International Journal of Biological Macromolecules, 132, 97-108. https://doi.org/10.1016/j.ijbiomac.2019.03.186
13. Andrews, S. H., Cheng, A., Stevens, H. Y., Logun, M. T., Webb, R. L., Jordan, E. T., Xia, B., Karumbaiah, L., Guldberg, R. E., & Stice, S. L. (2019). Chondroitin sulfate glycosaminoglycan scaffolds for cell and recombinant protein‐based bone regeneration. Stem Cells Translational Medicine, 8(4), 575-585.
14. Yuan, H., Li, X., Lee, M.-S., Zhang, Z., Li, B., Xuan, H., Li, W.-J., & Zhang, Y. (2020). Collagen and chondroitin sulfate functionalized bioinspired fibers for tendon tissue engineering application. International Journal of Biological Macromolecules. https://doi.org/10.1016/j.ijbiomac.2020.12.152