摘要:生物学家证明,HIV-1的衣壳就像特洛伊木马一样,通过核孔传递病毒货物。
逆转录病毒不能自己复制——它们必须将自己的遗传密码插入宿主的DNA中,利用宿主细胞的资源复制更多的自己,从而进一步感染。一些逆转录病毒仅在细胞分裂时感染细胞,此时保护宿主遗传物质的核膜破裂,使其易于接近。HIV-1是一种逆转录病毒,被称为慢病毒,可以感染非分裂细胞。
HIV-1通过将其基因组包装成一个被称为衣壳的大锥形结构将其传递到细胞核中,但其确切的机制几十年来一直难以捉摸。穿过核膜的过程是通过核孔(甜甜圈形状的蛋白质组合)进行的,并受其调节。人类细胞有大约2000个核孔穿过核膜。一些早期的证据表明,衣壳在进入细胞核的过程中保持完整,但这就产生了一个维度上的难题。HIV-1的锥形衣壳长约120纳米,宽约60纳米——研究人员认为,太大了,无法穿过只有43纳米宽的核孔。
麻省理工学院生物系施瓦茨实验室的成员对这个问题产生了兴趣,当时实验室里的一位博士后使用冷冻电子断层扫描,将冷冻细胞切片来检查结构,结果显示核膜上的核孔大于43纳米。事实证明,当它们离开它们的自然环境时,它们会收缩。在天然条件下,核孔复合物的宽度约为60纳米,足以容纳HIV-1衣壳。
知道了它可以适应,一个问题仍然存在:衣壳如何在密集的面条状蛋白质网络中穿行,这些蛋白质在核孔通道中起到筛子的作用?这种意大利面状的网状结构允许小货物通过,但阻止大货物进入,除非有一种叫做核运输受体的蛋白质护送。
在今天发表在《Nature》杂志上的一篇开放获取的论文中,研究人员提供了证据,证明HIV-1衣壳模仿细胞的运输受体穿过核孔。
 图1 HIV-1的衣壳像细胞的货物受体一样进入细胞核
图1 HIV-1的衣壳像细胞的货物受体一样进入细胞核
为了支持这一结论,研究人员在体外展示了三件事:HIV-1衣壳可以通过核孔类似物运送货物;衣壳可以与核孔通道中的蛋白质筛相互作用;在没有天然转运蛋白的情况下,衣壳会瞄准核孔。
核转运受体通过“赶走”通道内意大利面状的蛋白质网,护送大量货物通过核孔——就像有人牵着你的手,引导你穿过拥挤的舞池。HIV-1衣壳与意大利面样蛋白相互作用,但它的作用更像是特洛伊木马——衣壳封装病毒货物,保护它在细胞质中不被检测到,当它进入核孔复合体时。
“细胞真正令人惊奇的是,它们非常复杂。研究细胞的真正困难之处在于它们非常复杂,”Schwartz实验室的研究生、第一作者Erika Weiskopf开玩笑说。“生物化学家一直在努力寻找方法,在简化的背景下研究他们的系统,但仍然赋予它细胞生物学的味道。”
为此,Weiskopf实验室与马克斯普朗克多学科科学研究所细胞物流主任Dirk Görlich合作。Görlich是与麻省理工学院生物学教授托Thomas Schwartz共同撰写该论文的资深作者。Görlich的实验室已经在核孔中发现了浓缩的意大利面状蛋白质液滴,这些液滴允许和排除货物的方式与核孔相同。在实验中,荧光标记的货物没有进入液滴,但是包装在HIV-1衣壳中的荧光标记货物被递送。这表明衣壳可以通过核孔运送货物。
通过生物物理结合试验,研究人员还发现HIV-1衣壳与通道内的蛋白质相互作用。在不同的通道部分发现不同的意大利面样蛋白,例如在细胞质一侧的入口或仅在通道内;人类细胞中有10种这样的蛋白质。衣壳是一种混杂的粘合剂——它可以与通道中发现的所有意大利面状蛋白质相互作用。
即使没有细胞的转运受体,衣壳也能靶向核孔复合体,这表明它不征用天然转运受体来寻找和进入核孔。研究小组在核细胞质运输领域使用了一种经典的实验来收集证据:当细胞用洋地黄苷处理时,它们的膜变得多孔。细胞质中的所有物质都会从细胞中泄漏出来,但核膜将保持完整。尽管缺乏天然蛋白,衣壳被核孔复合物吸引,这一行为表明核转运受体。
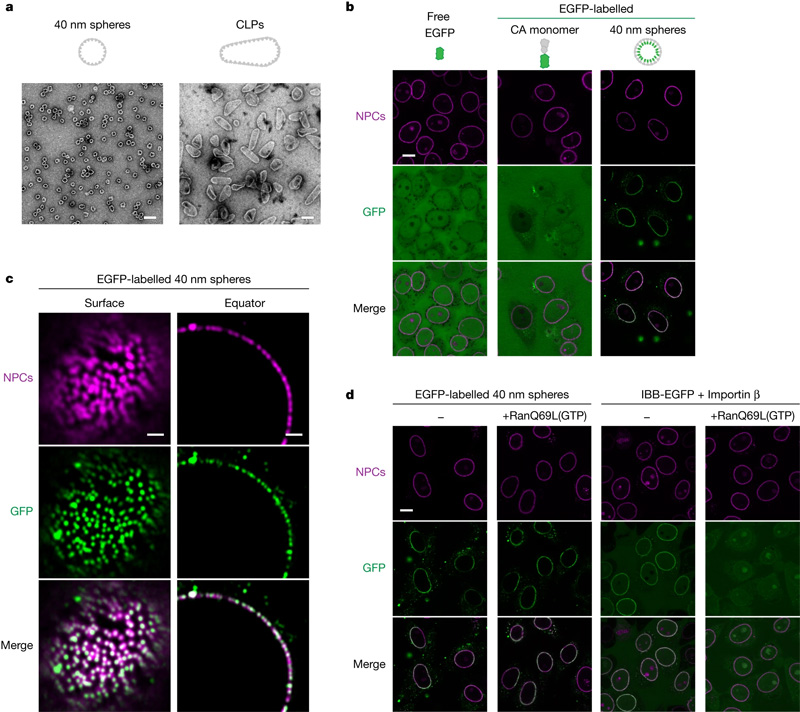 图2 HIV-1衣壳物种对NPC的自主靶向
图2 HIV-1衣壳物种对NPC的自主靶向尽管衣壳的行为像核转运受体一样穿透核孔,但它本质上是不同的。运输受体不需要像衣壳那样隐藏物质以避免被发现。
这些发现为研究核孔复合体能够容纳什么打开了新的思路。
Weiskopf说:“HIV-1衣壳是我们目前所知道的能够完整通过核孔复合体的最大的东西之一。这引发了各种各样的问题——还有什么我们认为不可能的东西可以通过这个孔?”
另一个问题是,人类细胞中的2000个核孔是否都是相同的,或者是否有什么东西使某些孔更容易让衣壳通过。
众所周知,衣壳具有不同寻常的弹性,这一特性可能是通过孔的关键。该领域另一个有趣的问题是,锥形衣壳是否通过挤压进入孔隙。
尽管该团队已经证明衣壳可以进入孔,但在通道的另一端发生的事情仍然未知-衣壳是否完全或部分进入细胞核或在通道内分解。Weiskopf正在研究干扰衣壳或意大利面状蛋白的部分,以了解哪些相互作用对成功进入衣壳最重要。
尽管这些结果扩大了我们对核孔的理解,但对于HIV-1感染和通过核孔复合物的转运过程仍有许多未知之处。
“核孔是细胞生物学中如此重要的一个元素,我们认为更好地理解它会很有趣——这就是我们如何发现核孔比我们预期的要大得多,”Weiskopf说。“我们肯定会尝试看看我们是否能理解HIV-1感染的机制,衣壳是如何在通道的另一边释放的,那里有什么重要的因素,以及你可以在多大程度上操纵或影响它用于治疗应用。”
参考资料
[1] HIV-1 capsids enter the FG phase of nuclear pores like a transport receptor